阿尔茨海默病新疗法可通过脑淋巴转运促进淀粉样蛋白清除
大脑中有数以千计的神经元在积极活动,它们通过放电组织人体的运动、思想和行为,这个行为也产生了大量的大脑垃圾。脑淋巴就是清除这些垃圾的重要系统。脑淋巴允许大脑周围的脑脊液进入动脉旁的血管周围空间,在这里脑脊液与神经元周围的间质液进行物质交换,包括各种离子、神经递质和调节分子、还有代谢垃圾,间质液中的废物可以通过静脉血管周围空间排出。这个过程中,星形胶质细胞表达的水通道蛋白4(Aquaporin 4, AQP4)是很关键的。星形胶质细胞会与血管形成接触面,在这个接触面上AQP4充当了水的通道。
2024年2月28日,Mitchell H. Murdock和Li-Huei Tsai等在Nature杂志上发表题为Multisensory gamma stimulation promotes glymphatic clearance of amyloid的新成果提供了阿尔茨海默病40Hz刺激疗法的新机制。该研究团队发现,40Hz多感官刺激能够促进AD小鼠脑脊液(CSF)和间质液(ISF)交换,加速淀粉样蛋白的淋巴清除。
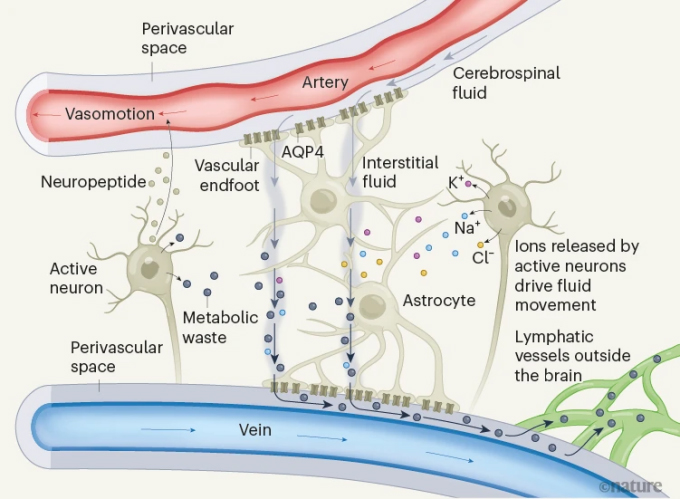
脑淋巴作用机制(图片来源:Nature)
研究人员在6个月大的5×FAD小鼠中进行实验,40Hz多感官刺激能够显著减少大脑淀粉样蛋白负荷。监测脑脊液动力学结果发现,40Hz刺激后,小鼠脑脊液流入和间质液外排显著增加。当研究者使用小分子抑制剂破坏AQP4功能,脑脊液流入减少、淀粉样蛋白负荷增加。显然,40Hz刺激真的可以促进淀粉样蛋白的淋巴清除。由于动脉血管运动能够调节脑脊液运动并且会被γ节律影响,研究者在小鼠前额叶皮层处固定了双光子成像,观测小鼠的动脉直径变化。在40Hz多感官刺激1小时后,小鼠动脉搏动显著增加,血管收缩幅度变大、频率也增快了,动脉的加速搏动显然会加速血管周围空间中脑脊液的流动。对刺激后的小鼠脑细胞进行单核RNA测序后,发现星形胶质细胞末端足上与脑脊液运输有关的钾通道Kcnk1表达增加;免疫组化分析也发现,AQP4极化增加。进一步分析发现,这一过程通过VIP神经元神经肽信号实现。
同期发表的另一篇论文则发现,睡眠和麻醉期间出现的神经元同步放电可以加速脑脊液灌注。虽然这项研究并未提及特定神经元活动频率的影响,但也不能排除不同大脑区域具有一个最佳频率的可能。无论如何,脑淋巴如何清除大脑垃圾,是会对包括AD在内多种神经退行性疾病产生影响的问题,如何能够有效利用这个清除系统,可以为治疗这类疾病带来新的思路。
原文链接:https://www.nature.com/articles/s41586-024-07132-6
关联产品:

